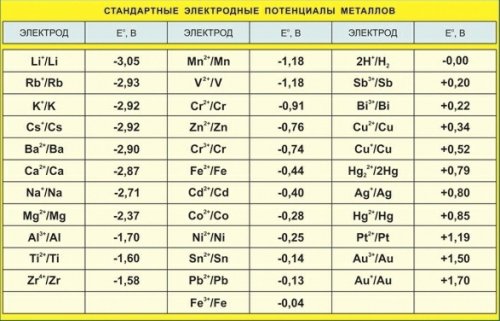
الیکٹروڈ کی صلاحیت کیا ہے؟
الیکٹروڈ پوٹینشل یا دھات کا الیکٹروڈ پوٹینشل ایک ممکنہ فرق ہے جو دھاتی حل کے انٹرفیس پر اس وقت ہوتا ہے جب ایک دھات کو ایک الیکٹرولائٹ محلول میں ڈبویا جاتا ہے جس کے نتیجے میں سطحی دھاتی آئن ایٹموں کے تعامل کے نتیجے میں کرسٹل جالی کے نوڈس میں قطبی الیکٹروڈ کی سطح پر مبنی پانی کے مالیکیولز... یہ ایک برقی ڈبل پرت کی تشکیل کی وجہ سے ہے، یعنی باؤنڈری پر چارج شدہ ذرات کی غیر متناسب تقسیم۔
الیکٹرولائٹس میں دھاتوں کی تحلیل کا رجحان بجلی کے کیمیائی ذرائع میں استعمال ہوتا ہے۔ دھات کی پلیٹ اپنے نمک کے محلول میں نوشی کی جاتی ہے، کسی نہ کسی طرح، اس میں گھل جاتی ہے۔ اس رجحان کو بعض اوقات دھات کی تحلیل لچک بھی کہا جاتا ہے۔
زنک سلفیٹ ZnTAKA4 کے محلول میں ڈوبی ہوئی زنک پلیٹ زنک کے ذرات کو مثبت چارج شدہ آئنوں کی شکل میں محلول میں دیتی ہے۔اس حقیقت کی وجہ سے کہ گلابی ایٹم مثبت چارج شدہ آئنوں کی صورت میں نکلتے ہیں، زنک پلیٹ پر مفت الیکٹران کی زیادتی بنتی ہے اور یہ منفی چارج ہو جاتا ہے، اور سطح کے قریب مائع کی تہہ میں مثبت آئنوں کی زیادتی بن جاتی ہے۔ زنک کی، اور اس وجہ سے یہ پرت مثبت طور پر بھری ہوئی ہے۔ اس طرح، مائع اور دھات کے درمیان انٹرفیس پر مخالف علامت کے مقامی طور پر الگ الگ چارجز کی ایک برقی ڈبل تہہ پیدا ہوتی ہے۔
یہ چارجز دھات کے حل میں مزید گزرنے کی مخالفت کریں گے — منفی پلیٹیں مثبت دھاتی آئن کو رکھتی ہیں، اور الیکٹرولائٹ کا مثبت چارج دھاتی آئن کو واپس پلیٹ کی طرف دھکیل دیتا ہے۔ دوسرے لفظوں میں، دھاتی مائع انٹرفیس پر ڈبل پرت کا برقی میدان دھاتی آئنوں کی محلول میں مزید منتقلی کا مقابلہ کرتا ہے۔ دھات کے محلول میں جانے کے رجحان کی قوتوں، فطرت میں کیمیائی، اور ایک توازن قائم ہوتا ہے۔ برقی قوتیں جو مخالف ہیں۔
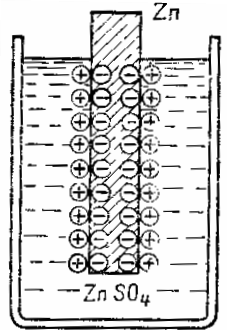
دھات اور الیکٹرولائٹ کے درمیان انٹرفیس پر برقی ڈبل پرت کی تشکیل کا خاکہ
اس طرح، الیکٹرولائٹ میں تحلیل ہونے کی وجہ سے، دھاتی الیکٹروڈ الیکٹرولائٹ کے حوالے سے ایک مخصوص الیکٹروڈ (دوسرے الفاظ میں، الیکٹرو کیمیکل) صلاحیت حاصل کرتا ہے، جو الیکٹرولائٹ کے مواد اور الیکٹرولائٹ کی ساخت پر منحصر ہوتا ہے۔
تاہم، الیکٹروڈ کی صلاحیت مثبت ہو سکتی ہے۔ یہ ان صورتوں میں ہوتا ہے جہاں محلول کے مثبت آئن الیکٹروڈ تک پہنچتے ہیں، اسے مثبت طور پر چارج کرتے ہیں، اور الیکٹرولائٹ کی تہہ - منفی طور پر، مثال کے طور پر، جب تانبے کی پلیٹ کو کافی مقدار میں کاپر سلفیٹ (CuSO)4) کے محلول میں ڈبو دیا جاتا ہے۔
الیکٹرک ڈبل پرت کو کپیسیٹر سے تشبیہ دی جا سکتی ہے، جس میں سے ایک پلیٹ دھات کی سطح ہے اور دوسری دھات کی سطح پر محلول میں آئنوں کی ایک تہہ ہے۔ مخالف چارج شدہ پلیٹوں کے درمیان اور ممکنہ طور پر ایک فرق، یا چھلانگ ہے۔
الیکٹروڈ سلوشن انٹرفیس پر ممکنہ چھلانگ سسٹم کی ریڈوکس صلاحیت کی پیمائش کے طور پر کام کر سکتی ہے۔ تاہم، اس طرح کی ممکنہ چھلانگ یا، مساوی طور پر، دونوں مراحل کے درمیان ممکنہ فرق کی پیمائش کرنا ناممکن ہے۔ لیکن آپ ای کی پیمائش کر سکتے ہیں۔ وغیرہ ج. الیکٹروڈز پر مشتمل عناصر جن میں ہم دلچسپی رکھتے ہیں اور کچھ ایک (تمام صورتوں میں ایک جیسا) الیکٹروڈ، جن کی صلاحیت کو مشروط طور پر صفر سمجھا جاتا ہے۔
اس کی پیمائش کی گئی ہے، وغیرہ۔ c. الیکٹروڈ کی ریڈوکس صلاحیت کو نمایاں کرے گا جس میں ہم کچھ مشروط صفر کے مقابلے میں دلچسپی رکھتے ہیں۔ اس طرح حاصل ہونے والی قدر کو دھات کی اندرونی صلاحیت کہا جاتا ہے۔
کسی بھی دھات کے الیکٹروڈ پوٹینشل کی پیمائش کرنے کے لیے، الیکٹرولائٹ میں دوسرا الیکٹروڈ رکھنا ضروری ہے، جس کے نتیجے میں اس کے مواد کے لحاظ سے ایک مخصوص الیکٹروڈ پوٹینشل ہوگا۔ لہذا، دو الیکٹروڈ پوٹینشل کے صرف الجبری مجموعے کو براہ راست ناپا جا سکتا ہے۔
اس وجہ سے، مختلف مواد کے الیکٹروڈ پوٹینشل کا تعین ایک معیار (ایک ہائیڈروجن الیکٹروڈ، جس کی صلاحیت کو عام طور پر صفر سمجھا جاتا ہے) کے حوالے سے کیا جاتا ہے۔
دیگر حوالہ جات الیکٹروڈ جن کی ممکنہ نسبت ہائیڈروجن اسٹینڈرڈ الیکٹروڈ کے بارے میں معلوم ہے بھی پیمائش کے لیے استعمال کیے جا سکتے ہیں۔ یہ صلاحیت بھی e کی پیمائش کی بنیاد پر پائی جاتی ہے۔ وغیرہ c. ایک منتخب حوالہ الیکٹروڈ اور معیاری ہائیڈروجن الیکٹروڈ پر مشتمل ایک سرکٹ۔
اگر معیاری ہائیڈروجن الیکٹروڈ سے منسلک مطالعہ شدہ الیکٹروڈ منفی ہے، تو علامت »-» اندرونی پوٹینشل پر تفویض کی جاتی ہے، بصورت دیگر، نشان «+»۔
مثال کے طور پر، زنک -0.76 V، کاپر +0.34 V، چاندی +0.8 V کا الیکٹروڈ پوٹینشل، اس طریقے سے متعلقہ دھاتی نمک کے محلول میں ماپا جاتا ہے، اس کا تعین -مثبت پر زیادہ منفی پوٹینشل کو گھٹا کر کیا جاتا ہے۔
اگر مختلف الیکٹروڈ پوٹینشل والی دو دھاتی پلیٹوں کو متعلقہ الیکٹرولائٹ میں رکھا جاتا ہے، مثال کے طور پر، سلفیورک ایسڈ (H2SO4) کے محلول میں زنک (Zn) اور تانبے (Cth)، تو ان پلیٹوں سے منسلک ایک وولٹ میٹر ان کے درمیان وولٹیج دکھائے گا۔ وہ 1 V سے قدرے زیادہ ہیں۔
یہ وولٹیج، اس معاملے میں e کہلاتا ہے۔ وغیرہ c. galvanic جوڑے، تانبے کے الیکٹروڈ پوٹینشل میں فرق کی وجہ سے ہو گا، جس میں ایک چھوٹی مثبت صلاحیت ہے، اور زنک، جس میں ایک اہم منفی صلاحیت ہے۔ ایسا آلہ سب سے آسان گالوانک سیل ہے - وولٹا سیل۔
galvanic سیل میں، کیمیائی توانائی برقی توانائی میں تبدیل ہوتی ہے اور اس کی مدد سے کیمیائی عمل کی توانائی کی وجہ سے برقی کام انجام دینا ممکن ہوتا ہے۔
ای کی پیمائش وغیرہ c. سیل سرکٹ میں کرنٹ کی عدم موجودگی میں galvanic خلیات کو پیدا کیا جانا چاہیے۔ دوسری صورت میں، ماپا e. وغیرہ s. اس قدر سے کم ہوگی جس کی وضاحت کی گئی ہے۔ دو الیکٹروڈ کے توازن پوٹینشل کے درمیان فرق… درحقیقت، الیکٹروڈز پر الیکٹرانوں کا ایک خاص ارتکاز توازن کی صلاحیت سے مطابقت رکھتا ہے: یہ جتنا زیادہ مثبت ہوگا، اتنا ہی زیادہ منفی ہوگا۔ اس کے مطابق، دوہری تہہ کے اس حصے کی ساخت جو محلول میں ہے بھی مختلف ہے۔
ای کی پیمائش وغیرہ کے ساتھموجودہ بہاؤ کے بغیر ایک سیل عام طور پر معاوضے کے طریقہ سے تیار کیا جاتا ہے۔ اسے لاگو کرنے کے لیے، آپ کے پاس کچھ ہونا ضروری ہے۔ معیاری ای وغیرہ کے ساتھ نام نہاد عام عنصر اس طرح کے معیار کے طور پر کام کرتا ہے۔ زیادہ تر عام طور پر وہ ویسٹن کا مرکری-کیڈیمیم نارمل عنصر استعمال کرتے ہیں، جیسے وغیرہ کے ساتھ جو 20 ° C پر 1.01830 V کے برابر ہے۔